Второй закон термодинамики. Энтропия.
Второй закон связан с понятием энтропии, являющейся мерой хаоса (или мерой порядка). Второй закон термодинамики гласит, что для вселенной в целом энтропия возрастает.
Существует два классических определения второго закона термодинамики:
Кельвина и Планка
- Клаузиуса
Не существует циклического процесса, который извлекает количество теплоты из резервуара при определенной температуре и полностью превращает эту теплоту в работу. (Невозможно построить периодически действующую машину, которая не производит ничего другого, кроме поднятия груза и охлаждения резервуара теплоты)
Не существует процесса, единственным результатом которого является передача количества теплоты от менее нагретого тела к более нагретому. (Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара)
Оба определения второго закона термодинамики опираются на первый закон термодинамики, утверждающий, что энергия убывает.
Второй закон связан с понятием энтропии (S) .
Энтропия порождается всеми процессами, она связана с потерей системы способности совершать работу. Рост энтропии - стихийный процесс. Если объем и энергия системы постоянны, то любое измение в системе увеличивает энтропию. Если же объем или энергия системы меняются, энтропия системы уменьшается. Однако, энтропия вселенной при этом не уменьшается.
Для того, чтобы энергию можно было использовать, в системе должны быть области с высоким и низким уровнями энергии. Полезная работа производится в результате передачи энергии от области с высоким уровнем энергии к области с низким уровнем энергии.
- 100% энергии не может быть преобразовано в работу
- Энтропия может вырабатываться, но не может быть уничтожена
Эффективность теплового двигателя
Эффективность теплового двигателя, действующего между двумя энергетическими уровнями, определена в пересчете на абсолютные температуры
η = (T h - T c) / T h = 1 - T c / T h
η = эффективность
T c = нижняя граница температуры (K)
Для того, чтобы достичь максимальной эффективности T c должна быть на столько низкой, на сколько это возможно. Чтобы эффект был 100% -м, T c должна равнятся 0 по шкале Kельвина. Практически это невозможно, поэтому эффективность всегда меньше 1 (менее 100%).
- Изменение энтропии > 0
Необратимый процесс - Изменение энтропии= 0
Двусторонний процесс (обратимый) - Изменение энтропии < 0
Невозможный процесс (неосуществимый)
Энтропия определяет относительную способность одной системы влиять на другую. Когда энергия двигается к нижнему энергетическому уровню, где уменьшается возможность влияния на окружающую среду, энтропия увеличивается.
Определение энтропии
Энтропия определяется как:
T = абсолютная температура (K)
Изменение энтропии системы вызвано изменением содержания темпла в ней. Изменение энтропии равно изменению темпла системы деленной на среднюю абсолютную температуру (T a):
Сумма значений (H / T) для каждого полного цикла Карно равна 0. Это происходит из-за того, что каждому положительному H противостоит отрицательное значение H.
- Тепловой цикл Карно
Цикл Карно— идеальный термодинамический цикл.
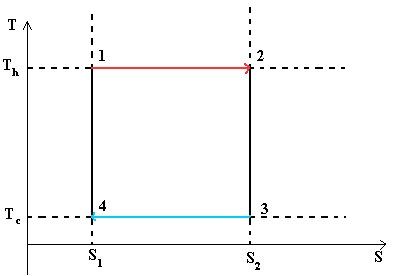
В тепловом двигателе, газ (реверсивно) нагревается (reversibly heated), а затем охлаждается. Модель цика следующая: Положение 1 --() --> Положение 2 --() --> Положение 3 --(изотермическое сжатие) --> Положение 4 --(адиабатическое сжатие) --> Положение 1
Положение 1 - Положение 2: Изотермическое расширение
Изотермическое расширение. В начале процесса рабочее тело имеет температуру T h , то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты Q H . При этом объём рабочего тела увеличивается. Q H =∫Tds=T h (S 2 -S 1) =T h ΔS
Положение 2 - Положение 3: Адиабатическое расширение
Адиабатическое (изоэнтропическое) расширение. Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника.
Положение 3 - Положение 4: Изотермическое сжатие
Изотермическое сжатие. Рабочее тело, имеющее к тому времени температуру T c , приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты Q c . Q c =T c (S 2 -S 1)=T c ΔS
Положение 4 - Положение 1: Адиабатическое сжатие
Адиабатическое (изоэнтропическое) сжатие. Рабочее тело отсоединяется от холодильника и сжимается без теплообмена с окружающей средой. При этом его температура увеличивается до температуры нагревателя.
При изотермических процессах температура остаётся постоянной, при адиабатических отсутствует теплообмен, а значит, сохраняется энтропия.
Поэтому цикл Карно удобно представить в координатах T и S (температура и энтропия).
Законы термодинамики были определены эмперическим путем (эксперементально). Второй закон термодинамики - это обощение экспериментов, связанных с энтропией. Известно, что dS системы плюс dS окружающей среды равно или больше 0.
- Энтропия адиабатически изолированной системы не меняется!
Пример - Энтропия при нагревании воды
Процесс нагревания 1 кг воды от 0 до 100 o C (273 до 373 K)
При 0 o C = 0 кДж/кг (удельная - на единицу массы)
При 100 o C = 419 кДж/кг
Изменение удельной энтропии:
dS = dH / T a
= ((419 кДж/кг) - (0 кДж/кг)) / ((273 К + 373 К)/2)
= 1.297 кДж/кг*К
Пример - Энтропия при испарении воды
Процесс превращения 1 кг воды при 100 o C (373 K) в насыщенный пар при 100 o C (373 K) при нормальных условиях.
Удельная энтальпия пара при 100 o C (373 K) до испарения = 0 кДж/кг
100 o C (373 K) при испарении = 2 258 кДж/кг
Изменение удельной энтропии:
dS = dH / T a
= (2 258 - 0) / ((373 + 373)/2)
= 6.054 кДж/кг*К
Полное изменение удельной энтропии испарения воды - это сумма удельной энтропии воды (при 0 o C) плюс удельная энтропия пара (при температуре 100 o C).
Первый закон термодинамики представляет собой закон сохранения энергии применительно к термодинамическим процессам: энергия не исчезает в никуда и не возникает из ничего, а лишь переходит из одного вида в другой в эквивалентных количествах. Примером может послужить переход теплоты (тепловой энергии) в механическую энергию, и наоборот.
Если к М
кг газа, занимающего объем V
(м 3)
при температуре Т
подвести при постоянном давлении некоторое количество теплоты dQ
, то в результате этого температура газа повысится на dT
, а объем – на dV
. Повышение температуры связано с увеличением кинетической энергии движения молекул dK
.
Увеличение объема сопровождается увеличением расстояния между молекулами и, как следствие, уменьшением потенциальной энергии dH
взаимодействия между ними. Кроме того, увеличив объем, газ совершает работу dA
по преодолению внешних сил.
Если, кроме указанных, никаких иных процессов в рабочем теле не происходит, то на основании закона сохранения энергии можно записать:
dQ = dK + dH + dA .
Сумма dK + dH
представляет собой изменение внутренней энергии dU
молекул системы в результате подвода теплоты.
Тогда формулу сохранения энергии для термодинамического процесса можно записать в виде:
dQ = dU + dA или dQ = dU + pdV .
Это уравнение представляет собой математическое выражение первого закона термодинамики : количество теплоты dQ , подводимое к системе газа, затрачивается на изменение ее внутренней энергии dU и совершение внешней работы dA .
Условно считают, что при dQ > 0 теплота сообщается рабочему телу, а при dQ < 0 теплота отнимается от тела. При dA > 0 система совершает работу (газ расширяется) , а при dA < 0 работа совершается над системой (газ сжимается) .
Для идеального газа, между молекулами которого нет взаимодействия, изменение внутренней энергии dU полностью определяется изменением кинетической энергии движения (т. е. увеличением скорости молекул) , а изменение объема характеризует работу газа по преодолению внешних сил.
Первый закон термодинамики имеет еще одну формулировку: энергия изолированной термодинамической системы остается неизменной независимо от того, какие процессы в ней протекают
.
Невозможно построить вечный двигатель первого рода, т. е. периодически действующую машину, которая совершала бы работу без затраты энергии.
Второй закон термодинамики
Первый закон термодинамики описывает количественные соотношения между параметрами термодинамической системы, имеющими место в процессах преобразования тепловой энергии в механическую и наоборот, но не устанавливает условия, при которых эти процессы возможны. Эти условия, необходимые для преобразования одного вида энергии в другой, раскрывает второй закон термодинамики.
Существует несколько формулировок этого закона, и каждая из них имеет одинаковое смысловое содержание. Здесь приведены наиболее часто упоминающиеся формулировки второго закона термодинамики.
1. Для превращения теплоты в механическую работу необходимо иметь источник теплоты и холодильник, температура которого ниже температуры источника, т. е. необходим температурный перепад.
2. Нельзя осуществить тепловой двигатель, единственным результатом действия которого было бы превращение теплоты какого-либо тела в работу без того, чтобы часть теплоты не передавалась другим телам.
Из этой формулировки можно сделать вывод, что невозможно построить вечный двигатель, совершающий работу благодаря лишь одному источнику теплоты, поскольку любой, даже самый колоссальный источник теплоты в виде материального тела не способен отдать тепловой энергии больше, чем ему позволяет энтальпия (часть полной энергии тела, которую можно превратить в теплоту, охладив тело до температуры абсолютного нуля)
.
3. Теплота не может сама по себе переходить от менее нагретого тела к более нагретому без затраты внешней работы.
Как видите, второй закон термодинамики не имеет в своей основе формулярнго содержания, а лишь описывает условия, при которых возможны те или иные термодинамические явления и процессы, подтверждая, по сути, общий закон сохранения энергии.
Один из основных законов физики, закон о неубывания энтропии в изолированной системе.
Для системы с постоянной температурой существует определенная функция состояния S - энтропия, которая определяется таким образом, что
1. Адиабатический переход из равновесного состояния A в равновесное состояние B возможен лишь тогда, когда
2. Прирост энтропии в медленном квазистатического процессе равно
Где T - температура.
Приведенное формулировка очень формаличне. Существует очень много альтернативных формулировок второго закона термодинамики. Например, Планк предложил следующую формулировку:
Невозможно построить машину, которая бы работала циклично, охлаждала бы источник тепла или поднимала вверх грузы, не вызывая
при этом никаких изменений в природе.
Константин Каратеодори дал аксиоматически строгое формулировки
Вблизи состояния 1 существуют такие состояния 2, адиабатические переходы от состояния 1 до состояния 2 невозможны.
Больцман сформулировал второй закон термодинамики с точки зрения статистической физики:
Природа стремится перейти из состояний с меньшей вероятностью реализации в состояния с большей вероятностью реализации.
Распространены такие формулировки.
Неможливо побудувати вічний двигун другого роду
.
Невозможно передать тепло от холодного тела к горячему, не затратив при этом энергию.
Каждая система стремится перейти от порядка к беспорядка.
Второй закон термодинамики был сформульваних в середине 19-го века, в те времена, когда создавалась теоретическая основа для конструирования и построения тепловых машин. Опыты Майера и Джоуля установили эквивалентность между тепловой и механической энергиями (первый закон термодинамики). Возник вопрос об эффективности тепловых машин. Экспериментальные исследования свидетельствовали о том, что часть тепла обязательно теряется при работе любой машины.
В 1850-х, 1860-х годах Клаузиус в ряде публикаций разработал понятие энтропии. В 1865 году он наконец выбрал для нового понятия имя. Эти публикации доказали также, что тепло невозможно полностью преобразовать в полезную работу, сформулировав таким образом второй закон термодинамики.
Статистическую интерпретацию второму закону термодинамики дал Больцман, введя новое определение для энтропии, которое базировалось на микроскопических атомистических представлениях.
Статистическая физика вводит новое определение энтропии, на первый взгляд очень отличное от определения термодинамики. Оно задается формулой Больцмана:
Где? - количество микроскопических состояний, соответствующих данному макроскопическому состояния, k B
- постоянная Больцмана.
Из статистического определения энтропии очевидно, что рост энтропии соответствует переходу к такому макроскопического состояния, которое характеризуется наибольшим значением микроскопических состояний.
Если исходное состояние термодинамической системы неравновесное, то со временем она переходит к равновесному состоянию, увеличивая свою энтропию. Этот процесс протекает только в одну сторону. Обратный процесс - переход от равновесного состояния к начальному неравновесного, не реализуется. То есть, течение времени получает направление.
Законы физики, описывающие микроскопический мир, инвариантные относительно замены t на-t. Данное утверждение справедливо как в отношении законов классической механики, так и законов квантовой механики. В микроскопическом мире действуют консервативные силы, нет трения, которое является диссипацией энергии, т.е. преобразованием других видов энергии в энергию теплового движения, а это в свою очередь связано с законом неубывания энтропии.
Представим себе, например, газ в резервуаре, помещенном в больший резервуар. Если открыть клапан меньшего резервуара, то газ через некоторое время заполнит больший резервуар таким образом, что его плотность выровняется. Согласно законам микроскопического мира, существует также и обратный процесс, когда газ из большего резервуара соберется в меньшую емкость. Но в макроскопическом мире такое никогда не реализуется.
Если энтропия каждой изолированной системе только увеличивается со временем, а Вселенная является изолированной системой, то когда-нибудь энтропия достигнет максимума, после чего любые изменения в нем станут невозможными.
Такие соображения, которые появились после установки второго закона термодинамики, получившие название тепловой смерти.
Эта гипотеза широко дискутировалась в 19-ом столетии.
Каждый процесс в мире приводит к рассеянию части энергии и перехода ее в тепло, ко все большему беспорядка. Конечно, наша Вселенная еще достаточно молод. Термоядерные процессы в звездах приводят к устойчивому потока энергии на Землю, например. Земля есть и еще долго будет оставаться открытой системой, которая получает энергию из различных источников: от Солнца, от процессов радиоактивного распада в ядре, т. В открытых системах, энтропия может уменьшаться, что приводит к появлению разнообразных благоустроенных стуктур.
Самопроизвольные (спонтанные) процессы описываются следующими характеристиками:
1. Все природные самопроизвольные процессы протекают в одном направлении, т. е. имеют одностороннее направление. Например, тепло от горячего тела переходит к холодному; газы стремятся занять наибольший объём.
2. Часть энергии переходит в теплоту, т. е. система из упорядоченного состояния переходит в состояние с беспорядочным тепловым движением частиц.
3. Самопроизвольные процессы можно использовать для получения полезной работы. По мере превращения система теряет способность производить работу. В конечном состоянии равновесия она имеет наименьший запас энергии.
4. Систему нельзя вернуть в исходное состояние, не производя каких-либо изменений в ней самой или в окружающей среде. Все самопроизвольные процессы термодинамически необратимы.
5. В самопроизвольном процессе начальное состояние является менее вероятным по сравнению с каждым последующим и наименее вероятным по сравнению с конечным.
Несамопроизвольные процессы протекают при затрате работы; при этом система удаляется от состояния равновесия (например, сжатие газа, электролиз).
Второй закон термодинамики - это постулат. Он имеет статистический характер и применим к системам из большого числа частиц.
Второй закон термодинамики имеет следующие формулировки:
1. Теплота не может переходить самопроизвольно от менее нагретого тела к более нагретому.
2. Невозможен процесс, единственным результатом которого является превращение теплоты в работу.
3. Вечный двигатель второго рода невозможен. Теплота, наиболее холодного из участвующих в процессе тел, не может служить источником работы.
Аналитическое выражение второго закона термодинамики и его обоснование с использованием цикла Карно . Суть выражения второго закона термодинамики - связь самопроизвольности процесса с ростом энтропии.Это выражение вытекает из рассмотрения вопроса о теоретической полноте превращения теплоты в работу в обратимом цикле Карно.
Цикл состоит из четырех процессов:
АВ - изотермическое расширение за счет теплоты Q 1, подведенной к газу при температуре Т 1 ;
ВС - адиабатическое расширение;
СД - изотермическое сжатие при температуре Т 2 , в этом процессе газ теряет теплоту Q 2 ;
ДА - адиабатическое сжатие до исходного состояния.
Теплота, поглощаемая (или выделяемая) при изотермическом расширении (или сжатии) одного моль идеального газа, равна работе
При адиабатическом расширении (или сжатии)
Применение этих уравнений к соответствующим процессам цикла приводит к выражению для термодинамического коэффициента полезного действия (к.п.д.):  . (4.3)
. (4.3)
Уравнение (4.3) является математическим выражением второго закона термодинамики.
Так как T 1 ‹ T 2 , то η ‹ 1.
Согласно теории Карно замена идеального газа любым другим веществом не приведет к изменению к.п.д. цикла Карно. Замена цикла Карно любым другим циклом приведет к меньшему к.п.д. (теорема Клазиуса-Карно). Таким образом, даже в случае идеальной тепловой машины превращение теплоты в работу не может быть полным.
Выражение второго закона термодинамики позволяет ввести понятие энтропии, с помощью которой сущность закона раскрывается в удобной и общей форме.
Изменим выражение (4.3):
 на
на  . (4.4)
. (4.4)
Отношение называется приведенной теплотой. Уравнение (4.4) показывает, что алгебраическая сумма приведенных теплот по обратимому циклу Карно равна нулю.
Для бесконечно малого обратимого цикла Карно 
где - элементарная приведенная теплота.
Любой цикл может быть заменен совокупностью бесконечно малых циклов Карно: .
В пределе эта сумма превратится в .
В теории интегралов доказывается, что если интеграл по замкнутому контуру равен нулю, то подинтегральное выражение есть полный дифференциал некоторой функции от параметров, определяющих состояние системы.
где S - это энтропия , такая функция состояния системы, полный дифференциал которой в обратимом процессе равен отношению бесконечно малого количества теплоты к температуре.
Понятие «энтропия» введено Клаузиусом (1850). Это выражение является математическим выражением второго закона термодинамики для обратимых процессов.
Изменение энтропии в обратимом процессе равно изменению энтропии в необратимом процессе, т.е. ![]() . Сравним теплоты обратимого и необратимого процессов. Согласно первому закону термодинамики
. Внутренняя энергия U
- это функция состояния системы, поэтому
. Сравним теплоты обратимого и необратимого процессов. Согласно первому закону термодинамики
. Внутренняя энергия U
- это функция состояния системы, поэтому ![]() . Максимальная работа совершается при обратимом процессе, поэтому
. Максимальная работа совершается при обратимом процессе, поэтому
В общем случае для обратимого и необратимого процессов второй закон термодинамики имеет следующее математическое выражение:
Здесь dS = const , а изменяется только правая часть уравнения, т.е. значение величины теплоты. Единицы измерения энтропии: [S ] = Дж/моль·К.
Объединенное уравнение первого и второго закона термодинамики:
Расчет изменения энтропии идеального газа.
Выразим изменение внутренней энергии ![]()
Разделив уравнение (4.6) на Т , определим изменение энтропии:
 (4.7)
(4.7)
Из уравнения идеального газа: следует, что . Тогда, после подстановки этого соотношения в (4.7):
 (4.8)
(4.8)
Проинтегрируем выражение (4.8) при и получим уравнение для расчета изменения энтропии идеального газа:
 (4.9)
(4.9)
Изотермический процесс , :  , (4.10)
, (4.10)
так как , то  . (4.11)
. (4.11)
Изохорический процесс, :  . (4.12)
. (4.12)
Изобарический процесс, :  . (4.13)
. (4.13)
Адиабатический процесс, : . (4.14)
Постулат Планка имеет следующую формулировку: при абсолютном нуле энтропия правильно образованных кристаллов чистых веществ равна нулю. Постулат позволяет рассчитать абсолютное значение энтропии, если известны теплоты фазовых переходов, и если известны теплоёмкости вещества в различных агрегатных состояниях.
Простая формулировка первого закона термодинамики может звучать примерно так: изменение внутренней энергии той или иной системы возможно исключительно при внешнем воздействии. То есть другими словами, чтобы в системе произошли какие-то изменения необходимо приложить определенные усилия извне. В народной мудрости своеобразным выражением первого закона термодинамики могут служить пословицы – «под лежачий камень вода не течет», «без труда не вытащишь рыбку из пруда» и прочая. То есть на примере пословицы про рыбку и труд, можно представить, что рыбка и есть наша условно закрытая система, в ней не произойдет никаких изменений (рыбка сама себя не вытащит из пруда) без нашего внешнего воздействия и участия (труда).
Интересный факт: именно первый закон термодинамики устанавливает, почему потерпели неудачу все многочисленные попытки ученых, исследователей, изобретателей изобрести «вечный двигатель», ведь его существование является абсолютно невозможным согласно этому самому закону, почему, смотрите абзац выше.
В начале нашей статьи было максимального простое определение первого закона термодинамики, в действительности в академической науке существует целых четыре формулировки сути данного закона:
- Энергия ни откуда не появляется и ни куда не пропадает, она лишь переходит из одного вида в другой (закон сохранения энергии).
- Количество теплоты, полученной системой, идет на совершение ее работы против внешних сил и изменение внутренней энергии.
- Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданной системе, и не зависит от способа, которым осуществляется этот переход.
- Изменение внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты, переданной системе, и работой, совершенной системой над внешними силами.
Формула первого закона термодинамики
Формулу первого закона термодинамики можно записать таким образом:
Количество теплоты Q, передаваемое системе равно суме изменения ее внутренней энергии ΔU и работы A.
Процессы первого закона термодинамики
Также первый закон термодинамики имеет свои нюансы в зависимости от проходящих термодинамических процессов, которые могут быть изохронными и изобарными, и ниже мы детально опишем о каждом из них.
Первый закон термодинамики для изохорного процесса
Изохорным процессом в термодинамике называют процесс, происходящий при постоянном объеме. То есть, если будь-то в газе или жидкости нагреть вещество в сосуде, произойдет изохорный процесс, так как объем вещества останется неизменным. Это условие имеет влияние и на первый закон термодинамики, проходящий при изохорном процессе.
В изохорном процессе объем V является константой, следовательно, газ работы не совершает A = 0
Из этого выходит следующая формула:
Q = ΔU = U (T2) – U (T1).
Здесь U (T1) и U (T2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
Первый закон термодинамики для изобарного процесса
Аналогично изобарным процессом называется термодинамический процесс, происходящий в системе при постоянном давлении и массе газа. Следовательно, в изобарном процессе (p = const) работа, совершаемая газом, выражается следующим уравнением первого закона термодинамики:
A = p (V2 – V1) = p ΔV.
Изобарный первый закон термодинамики дает:
Q = U (T2) – U (T1) + p (V2 – V1) = ΔU + p ΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0.
Применение первого закона термодинамики
Первый закон термодинамике имеет практическое применение к различным процессам в физике, например, позволяет вычислить идеальные параметры газа при разнообразных тепловых и механических процессах. Помимо сугубо практичного применение можно этому закону найти применение и философское ведь что ни говорите, но первый закон термодинамики является выражением одного из самых общих законов природы – закона сохранения энергии. Еще Еклезиаст писал, что ничто ни откуда не появляется и никуда не уходит, все пребывает вечно, постоянно трансформируясь, в этом и кроется вся суть первого закона термодинамики.
Первый закон термодинамики, видео
И в завершение нашей статьи вашему вниманию образовательное видео о первом законе термодинамике и внутренней энергии.



